ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕHИЯ
,
гетероциклы (от гетеро... и греч. kyklos - круг), органич. вещества, содержащие
цикл, в состав к-рого, кроме атомов углерода, входят атомы других элементов
(гетероатомы), наиболее часто N, О, S, реже - P, В, Si и др. Многообразие
типов Г. с. чрезвычайно велико, т. к. они могут отличаться друг от друга
числом атомов в цикле, природой, числом и расположением гете-роатомов,
наличием или отсутствием заместителей либо конденсированных циклов, насыщенным,
ненасыщенным или ароматич. характером гетероциклич. кольца. Неароматич.
Г. с. по хим. свойствам близки к своим аналогам с открытой цепью; нек-рые
различия обусловлены эффектами напряжения в цикле и пространственными эффектами,
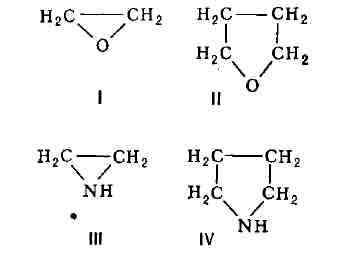
связанными с циклич. структурой. Так, окись этилена (I) и тетрагидрофуран
(II) подобны алифа-тич. эфиром простым, а этиленимин (III) и пирролидин
(IV) - алифатич. вторичным аминам:
Ароматичность проявляется
у Г. с. (гл. обр. 5- и 6-членных), содержащих, подобно другим ароматич.
соединениям, замкнутую систему 4n + 2n-электронов. Химия таких Г. с., сохраняя
известное сходство с химией ароматических соединений бензольного ряда,
определяется в основном специфич. характером каждого гетероциклич. ядра.
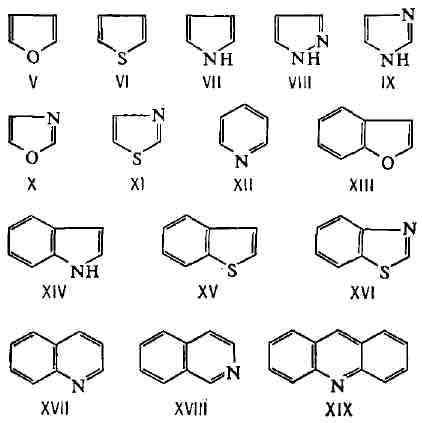
К важнейшим ароматич. Г. с. относятся фуран (V), тио-фен (VI), пиррол (VII),
пиразол (VIII), и.чидазол (IX), оксазол (X), тиазол (XI) и пиридин (XII).
Большое значение имеют также Г. с., конденсированные с бензольными ядрами,-
бензофуран (кумарон; XIII),
бензпиррол (.индол; XIV), бензтиофен (тионафтен; XV), бензтиазол (XVI),
оензпиридины - хинолин (XVII) и изохинолин (XVIII), дибензпиридин (акридин;
XIX):
Ароматич. характер фурана,
тиофена, пиррола и их бензпроизводных определяется участием неподелённой
электронной пары гетероатома в образовании замкнутой системы шести я-электронов.
В кислой среде гетероатом присоединяет протон и система перестаёт быть
ароматической. Поэтому такие Г. с., как фуран, пиррол и индол, не выдерживают
действия сильных кислот (тиофен устойчив к кислотам вследствие меньшего
сродства серы к протону):
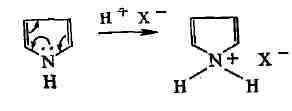
В 6-членных гетероциклах
неподелённая! электронная пара гетероатома не участвует в образовании ароматич.
системы связей. Поэтому пиридин - гораздо более сильное основание, чем
пиррол, и с кислотами образует устойчивые соли:
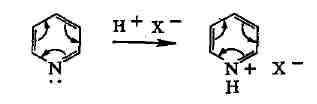
Нек-рые важные Г. с. могут
Роль Г. с. в процессах жизнедеятельности
Лит.: Каррер П., Курс органической
Б. Л. Дяткин.
А
Б
В
Г
Д
Е
Ё
Ж
З
И
Й
К
Л
М
Н
О
П
Р
С
Т
У
Ф
Х
Ц
Ч
Ш
Щ
Ъ
Ы
Ь
Э
Ю
Я
быть получены из каменноугольной смолы, напр, пиридин и его гомологи, хинолин,
изохинолин, индол, акридин, карбазол и др.; гидролизом растительных отходов
(шелуха подсолнечника, солома и т. п.) получают фурфурол. Однако наибольшее
значение имеют синтетич. методы, к-рые весьма разнообразны и специфичны;
они рассмотрены в статьях, посвящённых отдельным представителям Г. с. При
синтезе чаще всего исходят из соединений с открытой цепью. Для нек-рых
5-членных гете-роциклов известны взаимные превращения. Так, фуран, пиррол
и тиофен переходят друг в друга при действии соответственно H
растительных и животных организмов исключительно велика. К Г. с. относятся
такие вещества, как хлорофилл растений и гемин крови, компоненты
нуклеиновых кислот, коферменты,
нек-рые незаменимые аминокислоты (напр., пролин и триптофан), почти все
алкалоиды, пенициллин и нек-рые другие антибиотики, ряд витаминов, напр,
кобаламин (витамин B
широко применяемые в медицине синтетич. лекарственные вещества, такие,
как антипирин, амидопирин, анальгин, акрихин, амина-зин, норсульфазол и
другие. Г. с. широко применяют в различных отраслях промышленности (растворители,
красители, ускорители вулканизации каучука и т. д.).
химии, пер. с нем., Л., 1962, с. 955.